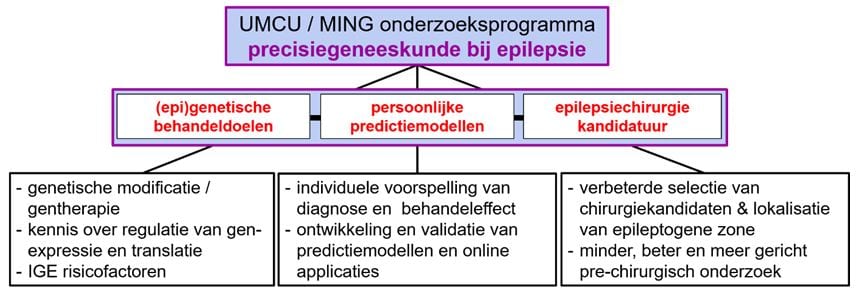
Precisiegeneeskunde bij epilepsie
Het onderzoeksprogramma ‘Preciesiegeneeskunde bij epilepsie’ van het UMC Utrecht is mede mogelijk gemaakt door een uitzonderlijke donatie van ouders met twee kinderen die epilepsie hebben. Het programma bouwt verder op het werk dat de afgelopen jaren door deze onderzoekers en hun teams is verricht, mede mogelijk gemaakt door een eerdere donatie van deze ouders in 2015. Beide donaties worden in de vorm van het zogenaamde MING fonds beheerd door de Stichting Vrienden van het UMC Utrecht.
Bij precisiegeneeskunde wordt rekening gehouden met de grote en kleine verschillen tussen mensen. Het is geneeskunde op maat. Dit is met name belangrijk voor mensen met een zeldzame vorm van epilepsie, bij wie de standaardbehandeling niet aanslaat. De epilepsie onderzoeksgroep van het UMC Utrecht wil de diagnostiek en behandeling van mensen met epilepsie verbeteren. Dit precisiegeneeskunde project heeft een persoonsgerichte benadering als uitgangspunt.